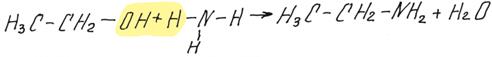Взаимодействие спиртов с галогенводородными кислотами осуществляются по механизму нуклеофильного замещения: отрицательная частица OH– замещается на нуклеофил Г–:
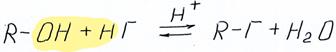
Рассмотрим примеры

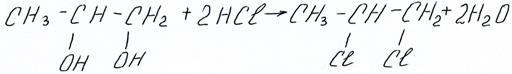
Данная реакция обратима – при добавлении раствора щелочи происходит гидролиз галогенпроизводного

Поэтому взаимодействие спирта с НГ следует проводить в присутствии серной кислоты.
https://youtu.be/8A9t7KiHjNA
В данной реакции спирт проявляет себя как очень слабое основание. Намного легче замена OH– на Г– происходит при реакциях спирта с галогенидами фосфора:

Эти реакции запоминать не нужно, но в тестовых заданиях галогениды фосфора (или смеси P + Г2) встречаются.
Дегидратация спиртов – реакции отщепления воды.
При нагревании спиртов с водоотнимающим агентом (чаще всего с концентрированной серной кислотой) происходит отщепление воды – дегидратация. В зависимости от способа отщепления воды возможно как образование простых эфиров, так и двойной связи (алкенов и циклоалкенов).
а) Дегидратация с образованием простых эфиров. В этом случае молекула воды «собирается» из двух групп –ОН:
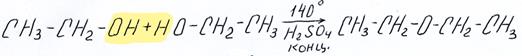
диэтиловый эфир
(этоксиэтан)
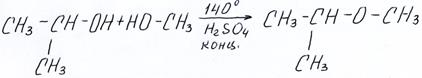
Метилизопропиловый эфир
(2-метоксипропан)
В этих реакциях простые эфиры образуются при т.н. межмолекулярной дегидратации – из одинаковых или разных молекул одноатомных спиртов.
Если спирт многоатомный, то вода может образоваться из двух гидроксильных групп одной молекулы, например с образованием циклического простого эфира
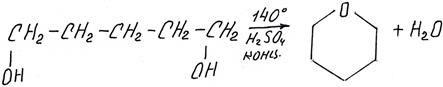
Дегидратация с образованием простых эфиров происходит при меньшей температуре (140°С), чем внутримолекулярная (180°С).
б) Внутримолекулярная дегидратация протекает с образованием двойной связи:
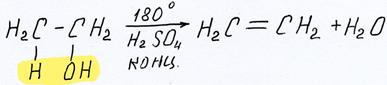
см. видео
https://youtu.be/m14SsmBqQSI
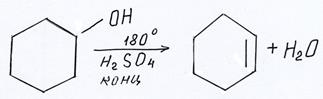
Дегидратация вторичных и третичных спиртов подчиняется правилу Зайцева – водород отщепляется от менее гидрогенизированного атома углерода:
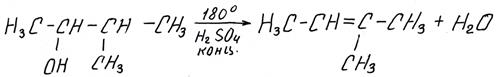
5. Дегидрирование (дегидрогенизация) спиртов – отщепление водорода. При пропускании паров спирта над раскаленным металлом (Cu, Ag, Ni, Pt, 300°С) от молекулы спирта отщепляется Н2.
Из первичных спиртов образуются альдегиды
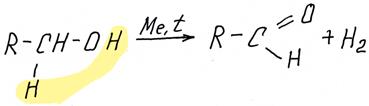
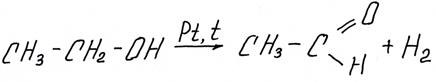
Из вторичных – кетоны
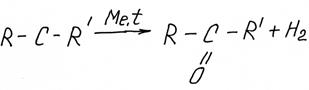
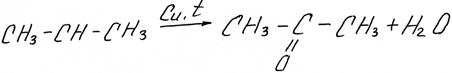
Третичные спирты не дегидрируются.
Окисление спиртов
а) Горение спиртов. Как и все органические вещества, спирты сгорают с образованием углекислого газа и воды.
https://youtu.be/f3LSEnhISOU
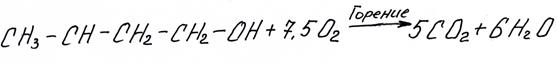
б) Неполное окисление спиртов. Под действием окислителей спирты переходят в карбонильные соединения. Продукт зависит от строения спирта и от силы окислителя.
Первичные спирты окисляются до альдегидов, которые, в свою очередь, могут окисляться до карбоновых кислот, приведем схему:
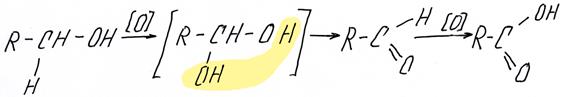
Надо запомнить, что спирты можно окислить не только KMnO4 и K2Cr2O7, но и пропуская пары спирта над раскаленным CuO. CuO является относительно слабым окислителем, он окислит спирты только до альдегидов (без дальнейшего образования кислот), приведем примеры реакций
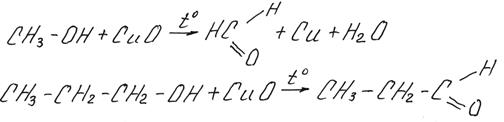
см. также видео
https://youtu.be/TSb3gN8i33w
Аналогично спирты окисляются кислородом в присутствии катализаторов (Cu, Cr2O3). Эти реакции распространены в промышленности, например:
см. также видео
https://youtu.be/4pXo7Z8tdZE
В жестких условиях окисления (растворы KMnO4 и K2Cr2O7) из первичного спирта можно получить как альдегид, так и кислоту. В тестовых заданиях будет указано что-то одно, в цепочках – можно ориентироваться по контексту.
Обычно считается, что спирты окисляются до соответствующих кислот, метанол окисляется до углекислого газа:
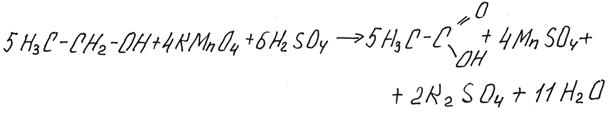
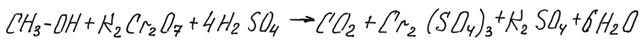
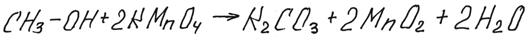
В последней реакции карбонат калия образуется по реакции
2КОН + СО2 = К2СО3 + Н2О
См. видео https://youtu.be/fIPd0vnqpx8
Вторичные спирты окисляются труднее, чем первичные, но всегда переходят в кетоны, в не зависимости от условий окисления:
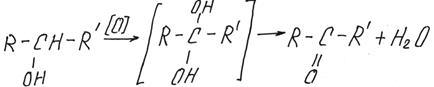
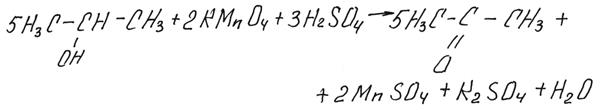
Третичные спирты устойчивы к окислению.
7. Синтез Лебедева – получение бутадиена из этанола.
При пропускании паров эанола при 400–450°С через оксидный катализатор (ZnO, MgO, SiO2, Al2O3) можно в одну стадию получить бутадиен-1,3:
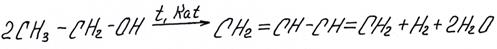
Эта реакция имела большое практическое значение, в ЕГЭ часто встречается и в тестах, и в цепочках.
8. Взаимодействие спиртов с аммиаком. При пропускании смеси паров спирта и аммиака над катализатором можно заменить группу –ОН на –NH2 и получить амины, например: