Неметаллы в бинарных соединениях проивляют нишую валентность (Na2S,HCl)
Металлы подгруппы А имеют валентность равную номеру группы
Составление химических формул по валентностям.
Оксид железа(2) Fe2O3
Хлорид кальция CaCl2
Алгоритм составления формул:
Записать химические элементы с конца названия вещества.
Раставить валентности.
Найти наименьшее общее кратное(НОК) между валентностями химических элементов
4.Находим индексы химических элементов:
НОК делим на валентность химических элементов.
Уравнения химических реакций.
4P+5O2=2P2O5
Алгоритм составления уравнений реакций:
1.Между реагентами ставим знак +
Ставим стрелку и записываем продукты реакции.
Уровняем количество атомов в реагентах и продуктах реакции,методом растоновки коэфицентов.
Na+O2=Na2O -схема реакции
Реагенты продукт реакции
4Na+O2=2Na2O
И 2 – коэфиценты
Н2,Сl2,O2,N2,Br2,I2,F2 капомнить
Типы химических реакций.
Mg+H2SO4=MgSO4+H2
KOH+H3PO4=K3PO4+H2O (реакция нейтрализации)

2Zn+O2=2ZnO -реакция соединения
СО2+Н2О=Н2СО3
Реакция соединения-это реакция между простыми веществами или сложными веществами,в результате которого образуется одно сложное вещество
(NH4)2Cr2O7=Cr2O3+N2+4H2O –реакция разложения
Реакция разложения-это реакция в которой из одного сложного вещества получается два или несколько простых или сложных веществ
FeCl2+Cu=CuCl2+Fe – реакция замещения
Реакция замещения-это реакция протекающая между простым и сложным веществами,при которых атомы простого вещества замещают атомы одного из элементов в сложном веществе.
HCl+NaOH=NaCl+H2O –Реакция обмена (реакция Нейтрализации(щелочь+кислота))
Реакция обмена-это реакция между сложными веществами.в которых они обмениваются своими составными частями.
Количество вещества.Моль.Молярная масса.
n-количество вещества «ню»-[моль]
n= 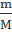
M-молярная масса
M= 
M-масса (грамм)
m=M*n
n(газа)=  (литр)
(литр)
V-обьем
V=Vm*n
Vm-молярный обьем (л/моль)
V(m)=22.4 л/моль при нормальных условиях
n= 
N=Na*n
Na=6.02*1023
Na-постоянная Авогадро
Показывает число частиц в 1 моле
Задача
Вычеслить количество вещества(n) Na2O в результате взаимодействия Na(2.3 моль) c O2
Дано: Решение:
n(Na)=2.3 моль 4Na+O2=2Na2O n(NaO)=2.3:2=1.15 моль
N(Na2O)-? х моль 2.3 моль Ответ:1.15 моль-n(Na2O)
Кислород.
Распространение в природе
1.В воздухе O2-21% N2-78%
В гидросфере(вода)
89% по массе 2Н2О=2Н2+О2
В Литосфере
49%
Живые и растительные организмы
65%
Способы получения:
Перегонка жидкого воздуха
Из кислородо содержащих веществ
2Н2О2=2Н2О+О2
2KClO3=2KCl+3O2
Кислород впервые был получен ученым Джоном Пристли 1 августа 1774 года.При накаливании HgO
О2-бесцветный газ,без вкуса и запаха,хорошо растворим в воде.
О2 при нагревании энергично реагирует со многими веществами,выделяется тепло и свет.Такие реакции называют реакциями горения.
Химические свойства

Простые вещества
С металломи
4Al+3O2=2Al2O3
С неметалломи
2Se+3O2=2SeO3
Сложные вещества
2H2S+O2 2H2O+2S
2H2O+2SO2
Тепловой эффект химических реакций.
Реакции идущие с выделением теплоты(энергии) называются экзотермические(наружу)