Для определения 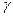 по формуле (26) необходимо измерить две величины
по формуле (26) необходимо измерить две величины  и
и 
- h1 - разности уровней в коленах манометра при установившемся давлении после накачивания воздуха;
- h2 - разности уровней после совершения адиабатического расширения и теплообмена с окружающей средой.
1. Накачивают с помощью насоса воздух в баллон так, чтобы разность уровней в коленах манометра была 250 – 280 мм. Выжидают 2 – 3 минуты (не меньше), чтобы падение давления полностью прекратилось. Кран 3 должен быть закрыт.
2. Отсчитывают разность уровней h1 с точностью до 1 мм.
Производят адиабатическое расширение. Для этого нажимают кнопку 4 и держат её нажатой 1 – 2 секунды.
3. Выжидают 2 – 3 минуты. Снимают новую разность уровней h2 также с точностью до 1 мм.
4. Те же измерения повторяют 5 раз. По формуле (26) вычисляют для каждого измерения показатель адиабаты. Все данные сводят в таблицу.
Таблица
| № опыта | Уровень в левом колене | Уровень в правом колене | h1, мм. | Уровень в левом колене | Уровень в правом колене | h2, мм. | γ |
Обработка результатов измерений
Результаты отдельных экспериментов будут отличаться друг от друга (случайный разброс), что приводит к появлению случайных погрешностей в определении 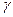 . Исключить случайные погрешности, так же и систематические погрешности, связанные с определением
. Исключить случайные погрешности, так же и систематические погрешности, связанные с определением  , нельзя. Они должны быть оценены для возможности критического анализа эксперимента. Точность эксперимента оценивают с помощью некоторой средней ошибки.
, нельзя. Они должны быть оценены для возможности критического анализа эксперимента. Точность эксперимента оценивают с помощью некоторой средней ошибки.
В теории вероятностей показывается, что ожидаемое значение такой средней ошибки  полн. следует вычислять по формуле:
полн. следует вычислять по формуле: 
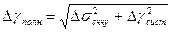 ,
,
где 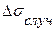 - случайная погрешность;
- случайная погрешность;
 - систематическая ошибка.
- систематическая ошибка.
Затем по формуле:  , где
, где 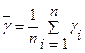 , рассчитывают относительную погрешность в определении
, рассчитывают относительную погрешность в определении  .
.
Рассмотрим вычисление 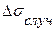 . Вопросами оценки случайных погрешностей занимается теория ошибок. Согласно этой теории, значение случайных погрешностей при большом
. Вопросами оценки случайных погрешностей занимается теория ошибок. Согласно этой теории, значение случайных погрешностей при большом  (число измерений) подчиняется статистической закономерности, которая называется законом распределения погрешностей.
(число измерений) подчиняется статистической закономерности, которая называется законом распределения погрешностей.
При определении 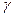 , как показывает эксперимент, таким законом распределения является закон Гаусса (нормальный закон). Согласно этому закону случайные погрешности не должны превышать значения некоторой предельной (случайной) погрешности, которая выражается в виде
, как показывает эксперимент, таким законом распределения является закон Гаусса (нормальный закон). Согласно этому закону случайные погрешности не должны превышать значения некоторой предельной (случайной) погрешности, которая выражается в виде
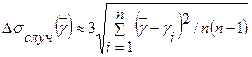 .
.
Случайные погрешности в определении 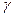 появляются за счет измерения
появляются за счет измерения  и связаны с тем, что практически невозможно осуществить в каждом опыте точного совпадения длительности открывания баллона со временем адиабатического расширения.
и связаны с тем, что практически невозможно осуществить в каждом опыте точного совпадения длительности открывания баллона со временем адиабатического расширения.
Погрешности в измерении  носят систематический характер и определяются ценой деления миллиметровой шкалы.
носят систематический характер и определяются ценой деления миллиметровой шкалы.
Систематическую погрешность находят по правилам отыскания погрешности для косвенных измерений по формуле
 ,
,
где 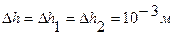 - систематическая погрешность при измерении
- систематическая погрешность при измерении 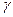 .
.
Пользуясь полученным числовым значением  , по формуле (17) оценивают число степеней свободы молекул воздуха.
, по формуле (17) оценивают число степеней свободы молекул воздуха.
Содержание и оформление отчёта по работе
Отчет по работе оформляется на отдельных листах в виде брошюры. В его содержание входят: название и цель работы, краткое изложение основных теоретических понятий, расчетная формула, таблица измерений, обработка их результатов, расчет относительной ошибки, значение числа степеней свободы с физическим истолкованием результата.
Вопросы для самопроверки
1. Что такое идеальный газ? Напишите уравнение состояния идеального газа.
2. Перечислите изопроцессы и законы, которым подчиняется газ в процессах. Изобразите изопроцессы в координатах P,V;P,T;V,T.
3. Что называется теплоемкостью, удельной и молярной теплоемкостью газа?
4. В чем состоит первое начало термодинамики?
5.Примените первое начало термодинамики к изохорическому и изобарическому процессам. Установите связь 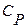 и
и 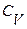 .
.
6. Что такое адиабатический процесс?
7. Разъясните физический смысл понятия числа степеней свободы.
8. Объясните связь между показателем адиабаты и числом степеней свободы.
9. Опишите установку и процессы, проходящие с выделенной частью воздуха в баллоне.
10. В каком порядке производятся измерения?
Литература
1. Детлаф А.А., Яворский Б.М. Курс физики: Учебное пособие для студентов втузов. М: Высшая физика 2000, 2001, 2002-718с.
2. Зисман Г.А., Тодес О.М. Курс общей физики: учебное пособие для студентов втузов. М: Наука 1974-336с.
3. Савельев И.В. Курс общей физики: учебное пособие для студентов втузов- М.: Наука, 1982.-432с. Кн.З.: молекулярная физика и термодинамика 1998.-208с.
4. Кикоин И.К. Кикоин А.К. Молекулярная физика. - М.: Наука, 1976,-480с.
5. Матвеев А.Н. Молекулярная физика. - М.: Высшая школа, 1987,-360с.
6. Евсеева Л.А.Методические указания к оформлению отчетов по лабораторным работам по физике, Саратов 1985.